1.Химические соединения


Блестящий металл натрий (Na) довольно мягкий и легко режется ножом. При контакте натрия со влажной кожей происходит моментальный взрыв. Хлор (Cl) - ядовитый, удушающий газ желтоватого цвета. Однако соединение с натрия с хлором - хлорид натрия (NaCl) - относительно безвредный усилитель вкуса, который мы знаем как поваренную соль. Сахар - ещё один пример химического соединения. Молекула сахара состоит из кислорода (O), водорода (H) и углерода (C). Чистый углерод входит в состав в ювелирных украшении и карандашей, водород используется как топливо для ракетных двигателей, газообразный кислород - один из компонентов воздуха. Но вместе они образуют сладкий белый кристаллический сахар.Химические и физические свойства соединений отличаются от свойств элементов их образующих.

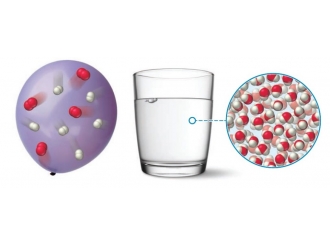
Не путайте химические соединения и смеси.В смесях элементы смешиваются в любых пропорцияхВ химическом соединении элементы соединяются в строго определённых пропорциях.Рассмотрим разницу между водородно-кислородной смесью и водой: Водородно-кислородная смесь может иметь любые пропорции газообразного водорода и кислорода. Вода, напротив, состоит из молекул воды, которые всегда содержат два атома водорода на каждый атом кислорода. Вода имеет определенное соотношение водорода к кислороду.

Соединения состоят из атомов, удерживаемых вместе химическими связями. Химические связи образуются из-за притяжения между заряженными частицами (электронами и протонами), из которых состоят атомы.Заряженные частицы действуют друг на друга электростатическими силами: одноименные заряды отталкиваются, а противоположные притягиваются. Эти силы ответственны за химическую связь.

Ковалентные связиКогда неметалл связывается с другим неметаллом, ни один из атомов не передает свой электрон другому. Вместо этого связывающие атомы делят часть своих электронов друг с другом. Ковалентно связанные атомы образуют молекулу, поэтому мы называем такие соединения молекулярными. Ионные связиМеталлы имеют тенденцию терять электроны, а неметаллы имеют тенденцию их приобретать. Следовательно, когда металл взаимодействует с неметаллом, он может передать один или несколько своих электронов неметаллу. Затем атом металла становится катионом (положительно заряженным ионом), а атом неметалла становится анионом (отрицательно заряженным ионом). Эти противоположно заряженные ионы притягиваются друг к другу электростатическими силами. Образуется ионное соединение, которое в твердом виде состоит из решетки — трехмерного массива чередующихся катионов и анионов.


CO2 — это химическая формула двуокиси углерода, который мы вдыхаем без какого-либо вреда для здоровья. CO2 используются растениями в важнейшем химическом процессе на планете – фотосинтезе.Если мы изменим индекс кислорода в формуле CO2, то получим соединение СО – угарный газ, являющийся опасным токсином. При вдыхании угарный газ нарушает способность крови переносить кислород, что может привести к летальному исходу. CO является основным веществом, ответственным за гибель людей, которые вдыхают слишком много автомобильных выхлопных газов. Нижние индексы для данного соединения никогда не меняются.

В химической формуле обычно указывают сначала наиболее металлические элементы. Поэтому формула поваренной соли — NaCl, а не ClNa. В соединениях, которые не включают металл, мы сначала пишем более металлоподобный элемент.
Написание химических формул


Некоторые химические формулы содержат группы атомов, которые действуют как единое целое. Например, соединение Mg(NO3)2 содержит один атом магния и две группы NO3. Часто группа атомов имеет заряд и называются многоатомными ионами. Например, (NO3)- - это многоатомный ион с зарядом 1-. Атомы внутри многоатомного иона связанны ковалентными связями. Между магнием и двумя нитратами (NO3)-
Посчитаем количество атомов в соединении Mg(NO3)2:Магний: 1 MgАзот: умножаем индекс за скобками на индекс внутри скобок 1 * 2 = 2 NКислорд: умножаем индекс за скобками на индекс внутри скобок 3 * 2 = 6 O
Расчет количества атомов в соединении

1.Молекулярная формула – это фактическое количество атомов каждого элемента в молекуле соединения.2. Эмпирическая — это простейшее целочисленное отношение атомов каждого элемента в соединении.Например, для углекислого газа молекулярная и эмпирическая формула будет СО2, так как единственное возможное соотношение углерода и кислорода в таких пропорциях. Для глюкозы молекулярная формула будет С6H12O6. Эмпирическая формула глюкозы - СH2O3. В структурной формуле используются линии для обозначения химических связей. Линии показывают, как атомы в молекуле связаны друг с другом.


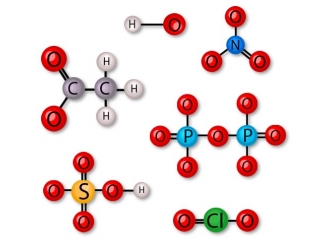
Как показывают атомы на рисунках (две модели):1.Шаро-стержневая модель показывает атомы в виде шариков, а химические связи — в виде стержней. Шарики и палочки соединены, образуя форму молекулы. Каждый шарик имеет свой цвет.2. Самая точная с научной точки зрения модель атома показывает шарики, заполняющие вокруг себя пространство (space-filling model). Такая модель показывает реальное расположение атомов и их размеры.




Комментариев пока нет